ประสิทธิภาพการยับยั้งและทำลายเซลล์มะเร็งปอดของ KERRA: วิเคราะห์เชิงลึกจาก A549, MTT, migration และ EGFR-driven models”
มะเร็งปอดเป็นหนึ่งในโรคมะเร็งที่รุนแรงและคร่าชีวิตผู้ป่วยมากที่สุดในโลกอย่างต่อเนื่อง แม้เทคโนโลยีทางการแพทย์จะก้าวหน้าไปมาก แต่สถิติการเสียชีวิตจากมะเร็งปอดยังคงอยู่ในระดับสูง และมีแนวโน้มเพิ่มขึ้นในหลายประเทศ โดยเฉพาะในเขตเมืองและพื้นที่ที่มีมลพิษทางอากาศรุนแรง ปัจจัยเสี่ยงของมะเร็งปอดในยุคปัจจุบันจึงไม่ได้จำกัดอยู่เพียงการสูบบุหรี่อีกต่อไป หากแต่ขยายไปสู่ปัจจัยสิ่งแวดล้อม เช่น ฝุ่นละอองขนาดเล็ก PM 2.5 ซึ่งได้รับการยอมรับในระดับสากลว่าเป็นสารก่อมะเร็งในมนุษย์
ปัญหาสำคัญของมะเร็งปอดคือ การตรวจพบที่ล่าช้า ผู้ป่วยส่วนใหญ่มักไม่มีอาการในระยะแรก และเมื่อเริ่มมีอาการก็มักอยู่ในระยะลุกลามแล้ว (ระยะที่ 3 หรือระยะที่ 4) ส่งผลให้อัตราการรอดชีวิตระยะ 5 ปีต่ำกว่า 10% แม้จะได้รับการรักษาด้วยยาเคมีบำบัด ยามุ่งเป้า หรือภูมิคุ้มกันบำบัดก็ตาม ความจริงข้อนี้สะท้อนอย่างชัดเจนว่า “การรักษาเมื่อเกิดโรคแล้ว” อาจไม่เพียงพอสำหรับการรับมือกับมะเร็งปอดในบริบทโลกปัจจุบัน ในเชิงชีววิทยา มะเร็งปอดไม่ได้เกิดขึ้นอย่างฉับพลัน แต่เป็นผลของกระบวนการสะสมความเสียหายระยะยาว โดยเฉพาะภาวะการอักเสบเรื้อรังระดับต่ำ (chronic low-grade inflammation) ภาวะ oxidative stress และแรงคัดเลือกที่เอื้อต่อการกระตุ้นสัญญาณการเจริญเติบโตของเซลล์ผ่านแกน EGFR–MAPK–NF-κB ซึ่งเป็นกลไกสำคัญของมะเร็งปอดชนิด adenocarcinoma และพบได้บ่อยในผู้ที่สัมผัส PM 2.5 อย่างต่อเนื่องในชีวิตประจำวัน
ด้วยเหตุนี้ แนวคิดด้าน “การป้องกันมะเร็งเชิงกลไก” (mechanism-based chemoprevention) จึงได้รับความสนใจเพิ่มขึ้นอย่างมากในงานวิจัยสมัยใหม่ แนวทางดังกล่าวมุ่งลดแรงขับทางชีววิทยาที่ก่อให้เกิดมะเร็งตั้งแต่ระยะก่อนเกิดโรคเต็มรูปแบบ แทนที่จะรอให้เกิดการกลายพันธุ์และการลุกลามของเซลล์มะเร็งแล้วจึงเข้ารักษาในระยะที่โรคลุกลาม
สมุนไพรตำรับ KERRA ถูกพัฒนาขึ้นภายใต้กรอบแนวคิดนี้ โดยมีหลักฐานเชิงทดลองสนับสนุนอย่างเป็นระบบว่า KERRA สามารถยับยั้งกระบวนการสำคัญที่เกี่ยวข้องกับการเกิดและการลุกลามของมะเร็งปอดได้หลายระดับพร้อมกัน ทั้งการลดการเพิ่มจำนวนของเซลล์มะเร็งปอดชนิด EGFR-positive การยับยั้งการเคลื่อนที่และการลุกลามของเซลล์ การยับยั้งเอนไซม์ EGFR-tyrosine kinase ทั้งในรูปแบบปกติและแบบกลายพันธุ์ ตลอดจนการลดระดับ reactive oxygen species (ROS) และการกดสวิตช์การอักเสบผ่าน NF-κB ซึ่งเป็นแกนกลางที่เชื่อมโยง PM 2.5 เข้ากับการเกิดมะเร็งปอด
การทดสอบการยับยั้งการเพิ่มจำนวนของเซลล์มะเร็งปอด (Anti-proliferation)
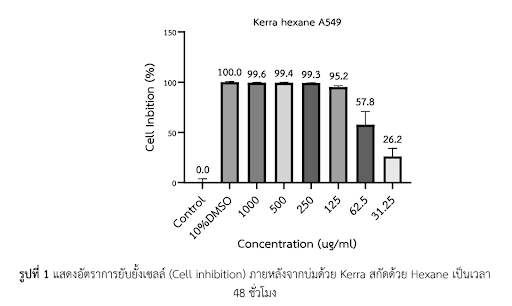
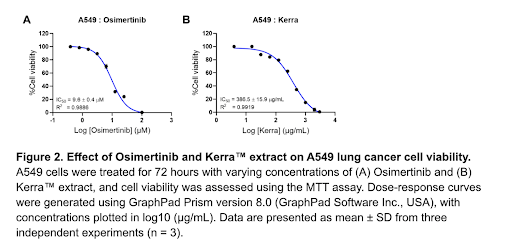
การทดลอง MTT cell viability assay ในเซลล์มะเร็งปอดชนิด A549 (EGFR-positive lung adenocarcinoma) แสดงให้เห็นว่า KERRA ลดการมีชีวิตรอดของเซลล์แบบ dose-dependent เมื่อบ่ม 72 ชั่วโมง โดยมีค่า IC₅₀ ~386.5 ± 15.9 µg/mL ภายใต้เงื่อนไขการทดลองมาตรฐาน
การตีความเชิงกลไก
รูปแบบการลด viability ของ KERRA ไม่ใช่ cytotoxic เฉียบพลัน แต่เป็นการ “กดการเติบโต” (growth suppression) ลักษณะนี้สอดคล้องกับการยับยั้งสัญญาณการแบ่งตัว (เช่น EGFR–MAPK) มากกว่าการทำลายโครงสร้างเซลล์โดยตรง คุณสมบัติดังกล่าวเหมาะกับบทบาท chemoprevention / growth modulation ในบริบท PM 2.5 ที่ความเสี่ยงเกิดจากแรงกดดันเรื้อรัง
การยับยั้งการเคลื่อนที่และการลุกลามของเซลล์ (Anti-migration / Anti-metastatic potential)
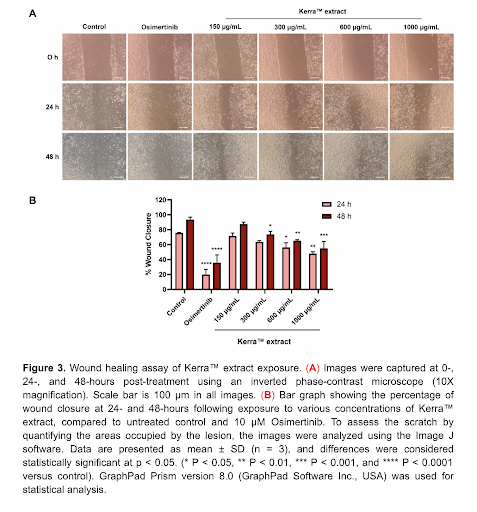
การทดสอบ scratch wound healing assay ใน A549 แสดงว่า KERRA ลดอัตราการปิดแผล (wound closure) อย่างมีนัยสำคัญ
และเป็นไปตามขนาดยา:
ที่ 24 ชั่วโมง: อัตราการปิดแผลลดลงต่อเนื่องเมื่อเพิ่มความเข้มข้น
ที่ 48 ชั่วโมง: แนวโน้มการลดลงยังคงชัดเจน แสดงการยับยั้งการเคลื่อนที่ของเซลล์
การตีความเชิงกลไก
การเคลื่อนที่ของเซลล์มะเร็งสัมพันธ์กับ EGFR–MAPK–NF-κB และโครงสร้างไซโตสเกเลตอน การลด migration บ่งชี้ว่า KERRA มีศักยภาพ ลดความสามารถการลุกลามและการแพร่กระจาย ซึ่งเป็นสาเหตุการเสียชีวิตหลักของมะเร็งปอด ในบริบท PM 2.5 การยับยั้ง migration คือการลด “ผลปลายทาง” ของสนามอักเสบที่เอื้อต่อ metastasis
การยับยั้ง EGFR-Tyrosine Kinase: แตะแกนมะเร็งโดยตรง
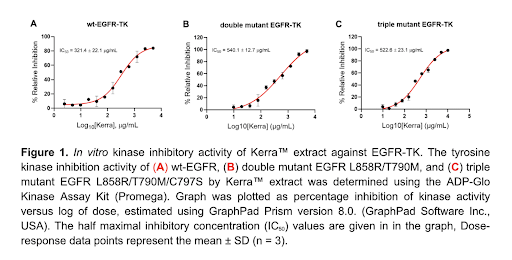
การทดสอบ ADP-Glo™ kinase assay แสดงว่า KERRA ยับยั้ง EGFR-TK ได้ทั้ง Wild-type EGFR Double-mutant (L858R/T790M) Triple-mutant (L858R/T790M/C797S) แม้ค่า IC₅₀ จะสูงขึ้นใน mutant forms แต่การที่ฤทธิ์ยังคงตรวจพบได้มีนัยสำคัญเชิงป้องกัน: PM 2.5 สร้างแรงกดดันที่คัดเลือกเซลล์พึ่งพา EGFR การยับยั้ง EGFR ตั้งแต่ระยะก่อนเกิดมะเร็งเต็มรูปแบบช่วย ลด selection pressure ต่อคลอนผิดปกติ แตกต่างจาก EGFR-TKI สังเคราะห์ที่มุ่งเป้าเดียวและดื้อยาได้ง่าย
การทำลาย/กดการอยู่รอดของเซลล์ผ่านสมดุล Apoptosis–Survival
ข้อมูลจาก proteomics และ FTIR สนับสนุนว่า KERRA ปรับสมดุลชีวโมเลกุลในเซลล์มะเร็ง: ลดสัญญาณ cell survival ที่เชื่อมกับการอักเสบเรื้อรัง เปลี่ยนโครงสร้างโปรตีนรอง (secondary structure) และโปรไฟล์ลิพิด/กรดนิวคลีอิก สร้าง biochemical signature ที่ต่างจากยามุ่งเป้าเดี่ยว เช่น EGFR-TKI)
การตีความ
KERRA ไม่ได้ “บังคับฆ่า” เซลล์ แต่ ปรับโหมดการทำงาน ของเซลล์ให้สูญเสียความได้เปรียบเชิงมะเร็ง แนวทางนี้ลดความเสี่ยงดื้อยาและเหมาะกับการใช้ระยะยาวเพื่อป้องกันผลของ PM 2.5
การลด ROS และการกดสวิตช์อักเสบ: เสริมฤทธิ์ต้านมะเร็ง
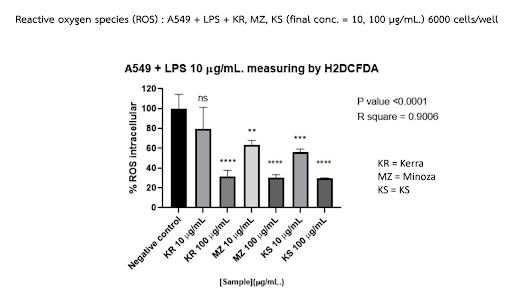
การลด ROS ใน A549 ภายใต้สภาวะอักเสบจำลอง และการกด NF-κB (p65) ในระดับโปรตีน ชี้ว่า KERRA:ลด DNA damage burden สัญญาณที่เชื่อมการอักเสบกับการอยู่รอด/การแบ่งตัวของเซลล์ ทำให้การยับยั้ง proliferation และ migration มีความยั่งยืนเชิงชีววิทยา
สรุปเชิงประสิทธิภาพ (Efficacy Summary)
หลักฐานจากทุกการทดลองชี้สอดคล้องกันว่า KERRA: ลดการเพิ่มจำนวน ของเซลล์มะเร็งปอด (growth suppression) ลดการเคลื่อนที่/ลุกลาม ของเซลล์ (anti-migration) ยับยั้ง EGFR-TK ทั้ง WT และ mutant ปรับสมดุล apoptosis–survival ผ่านการเปลี่ยนแปลงชีวโมเลกุล ลด ROS และกด NF-κB เสริมฤทธิ์ต้านมะเร็งในบริบท PM 2.5
ข้อสรุปจากงานวิจ้ย
ประสิทธิภาพของ KERRA ต่อเซลล์มะเร็งปอดไม่ได้จำกัดที่การทำลายเซลล์ แต่ครอบคลุมการ “กดสัญญาณและพฤติกรรมมะเร็ง” หลายมิติพร้อมกัน จึงเหมาะกับการป้องกันและชะลอผลของ PM 2.5 ในระยะยาว
การวิเคราะห์เชื่อมโยงกลไกกับผล Proteomics ของ KERRA
จากโมเดลปอดอักเสบสู่สนามก่อมะเร็ง (tumor-promoting field)
โมเดลปอดอักเสบที่ใช้ในงานทดลอง (เช่น macrophage RAW264.7 + LPS และ A549 + LPS) สะท้อน “สนามชีวภาพ” ที่ใกล้เคียงกับสถานการณ์จริงของการสัมผัส PM 2.5 ในชีวิตประจำวัน กล่าวคือเกิดการอักเสบระดับต่ำแต่ต่อเนื่อง (low-grade chronic inflammation) ROS/RNS overload การเปิดสวิตช์กลาง ของสัญญาณอักเสบ (NF-κB/MAPK) แรงคัดเลือก ให้เซลล์ที่พึ่งพาสัญญาณการเจริญเติบโตอยู่รอดและขยายตัว สนามลักษณะนี้ไม่จำเป็นต้องทำให้เกิดมะเร็งทันที แต่ทำหน้าที่ เร่งการสะสมความเสียหาย และ คัดเลือกคลอนผิดปกติ ในระยะยาว ซึ่งอธิบายได้ว่าทำไม PM 2.5 จึงเป็น tumor promoter ที่ทรงพลัง
หลักฐานเชิงหน้าที่: KERRA “ตัดวงจร” สนามก่อมะเร็งตั้งแต่ต้นน้ำ
เมื่อพิจารณาผลการทดลองเชิงหน้าที่ร่วมกัน จะเห็นรูปแบบเดียวกันอย่างสอดคล้อง: ต้นน้ำ (macrophage-driven inflammation): KERRA ลด NO และ IL-6 ลงใกล้ระดับปกติ ทำให้ลดไฟอักเสบที่เลี้ยงสนามก่อมะเร็ง กลางน้ำ (oxidative stress): KERRA ลด ROS ในเซลล์ปอดแบบ dose-dependent เกิดการลด DNA damage burden และการเปิดสวิตช์ NF-κB/MAPK ปลายน้ำ (growth signaling): KERRA ยับยั้ง EGFR-TK (ทั้ง WT และ mutant) → ลดการเพิ่มจำนวนและการเคลื่อนที่ของเซลล์ การทำงานแบบหลายจุดพร้อมกันนี้ทำให้ แรงขับของสนามก่อมะเร็งอ่อนกำลังลง ไม่ว่าจะเป็นการอักเสบ การแบ่งตัว หรือการลุกลาม
มุมมองโปรตีโอมิกส์: การปรับเครือข่าย ไม่ใช่การกดปุ่มเดียว
ข้อมูลโปรตีโอมิกส์และ FTIR สนับสนุนแนวคิดว่า KERRA เป็น network modulator มากกว่ายาที่กดเป้าหมายเดียว โดยพบการเปลี่ยนแปลงในกลุ่มโปรตีน/สัญญาณที่เกี่ยวข้องกับ การอักเสบและภูมิคุ้มกัน (ลดสัญญาณ pro-inflammatory) การตอบสนองต่อ oxidative stress (ฟื้นสมดุล antioxidant–pro-oxidant) สมดุลการอยู่รอด–การตายของเซลล์ (ลด survival bias ของเซลล์ผิดปกติ) โครงสร้างและการเคลื่อนที่ของเซลล์ (ลดศักยภาพการแพร่กระจาย) ภาพรวมจากโปรตีโอมิกส์จึงอธิบายได้ว่าเหตุใดผลเชิงหน้าที่ (ลด NO/ROS/IL-6, กด NF-κB, ลด migration) จึง “ยืนระยะ” และไม่ย้อนกลับง่าย แม้ใช้ความเข้มข้นที่ไม่ก่อพิษ
การเชื่อม EGFR–MAPK กับ PM 2.5: ลด selection pressure ก่อนการกลายพันธุ์
PM 2.5 ไม่จำเป็นต้องทำให้เกิดการกลายพันธุ์ใหม่เสมอไป แต่สร้าง selection pressure ให้เซลล์ที่พึ่งพา EGFR–MAPK อยู่รอดและขยายตัว การที่ KERRA ลดสัญญาณอักเสบที่ไปเสริม EGFR ทางอ้อม และ ยับยั้ง EGFR-TK โดยตรง จึงมีผลเชิงระบบคือ ลดแรงคัดเลือกก่อนที่คลอนกลายพันธุ์จะครองสนาม นี่คือหัวใจของการป้องกันเชิงกลไก (pre-mutation / pre-selection intervention)
จาก “การทดลอง” สู่ “การป้องกันในโลกจริง”
เมื่อถอดบทเรียนจากงานทดลองทั้งหมด แนวคิดการป้องกันจาก PM 2.5 ที่สอดคล้องกับชีววิทยาคือ ลดการอักเสบเรื้อรังอย่างต่อเนื่อง (ไม่ใช่เฉพาะช่วงค่าฝุ่นพุ่ง) ลด ROS และภาระความเสียหายต่อ DNA ในระยะยาว ลดการพึ่งพาสัญญาณการเจริญเติบโตผิดปกติ (EGFR/MAPK) ใช้เครื่องมือที่ ปลอดภัย ใช้ได้นาน และไม่กดระบบใดระบบหนึ่งเกินไป หลักฐานจากโมเดลปอดอักเสบ + โปรตีโอมิกส์ชี้ว่า KERRA ตอบโจทย์ทั้ง 4 ข้อนี้พร้อมกัน
บทสรุป
สมุนไพรตำรับ KERRA มีหลักฐานเชิงทดลองสนับสนุนอย่างเป็นระบบว่า KERRA สามารถยับยั้งกระบวนการสำคัญที่เกี่ยวข้องกับการเกิดและการลุกลามของมะเร็งปอดได้หลายระดับพร้อมกัน ทั้งการลดการเพิ่มจำนวนของเซลล์มะเร็งปอดชนิด EGFR-positive การยับยั้งการเคลื่อนที่และการลุกลามของเซลล์ การยับยั้งเอนไซม์ EGFR-tyrosine kinase ทั้งในรูปแบบปกติและแบบกลายพันธุ์ ตลอดจนการลดระดับ reactive oxygen species (ROS) และการกดสวิตช์การอักเสบผ่าน NF-κB ซึ่งเป็นแกนกลางที่เชื่อมโยง PM 2.5 เข้ากับการเกิดมะเร็งปอด
อ้างอิง
- Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71(3):209–249.
- Bray F, Laversanne M, Weiderpass E, Soerjomataram I. The ever-increasing importance of cancer as a leading cause of premature death worldwide. Cancer. 2021;127(16):3029–3030.
- World Health Organization. Outdoor air pollution. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Volume 109. Lyon: IARC; 2016.
- Turner MC, Krewski D, Diver WR, Pope CA 3rd, Burnett RT, Jerrett M, et al. Ambient air pollution and cancer mortality in the Cancer Prevention Study II. Environ Health Perspect. 2017;125(8):087013.
- Cohen AJ, Brauer M, Burnett R, Anderson HR, Frostad J, Estep K, et al. Estimates and 25-year trends of the global burden of disease attributable to ambient air pollution. Lancet. 2017;389(10082):1907–1918.
- Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2023. CA Cancer J Clin. 2023;73(1):17–48.
- Herbst RS, Morgensztern D, Boshoff C. The biology and management of non–small cell lung cancer. Nature. 2018;553(7689):446–454.
- Paez JG, Jänne PA, Lee JC, Tracy S, Greulich H, Gabriel S, et al. EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science. 2004;304(5676):1497–1500.
- Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation. Cell. 2011;144(5):646–674.
- Reuter S, Gupta SC, Chaturvedi MM, Aggarwal BB. Oxidative stress, inflammation, and cancer: how are they linked? Free Radic Biol Med. 2010;49(11):1603–1616.
- Klaunig JE, Kamendulis LM. The role of oxidative stress in carcinogenesis. Annu Rev Pharmacol Toxicol. 2004;44:239–267.
- Balkwill F, Mantovani A. Inflammation and cancer: back to Virchow? Lancet. 2001;357(9255):539–545.
- Zhang J, Wang X, Vikash V, Ye Q, Wu D, Liu Y, et al. ROS and ROS-mediated cellular signaling. Oxid Med Cell Longev. 2016;2016:4350965.
- Liu Y, Zhang X, Han C, Wan G, Huang X, Ivan C, et al. TP53 loss creates therapeutic vulnerability in colorectal cancer.
- Nature. 2015;520(7549):697–701.
- Gupta SC, Patchva S, Aggarwal BB. Therapeutic roles of curcumin: lessons learned from clinical trials. AAPS J. 2013;15(1):195–218.
- Surh YJ. Cancer chemoprevention with dietary phytochemicals. Nat Rev Cancer. 2003;3(10):768–780.
- Kensler TW, Spira A, Garber JE, Szabo E, Lee JJ, Dong Z, et al. Transforming cancer prevention through precision medicine and immune-oncology. Cancer Prev Res. 2016;9(1):2–10.