PM 2.5 อันตรายกว่าที่คิด—ต้นเหตุปอดอักเสบ มะเร็งปอด และแนวทางป้องกันผลกระทบเชิงสมุนไพร
PM 2.5 เป็นปัญหาสุขภาพระดับประเทศและระดับโลกอย่างแท้จริง โดยเฉพาะในเขตเมืองและพื้นที่อุตสาหกรรม ปัญหา PM 2.5 ไม่ได้ส่งผลแค่ระยะสั้นอย่างไอ แสบคอ หรือหายใจไม่สะดวก แต่เป็นตัวกระตุ้น ปอดอักเสบเรื้อรัง, ปอดอุดกั้นเรื้อรัง (COPD) และเพิ่มความเสี่ยง ก่อมะเร็ง โดยเฉพาะ มะเร็งปอด ในคนไม่สูบบุหรี่ ผ่านกลไกการอักเสบเรื้อรังและอนุมูลอิสระที่ทำลายเซลล์ปอดอย่างต่อเนื่อง ในช่วงหลายปีที่ผ่านมา หลักฐานทางวิทยาศาสตร์ชี้ชัดว่า PM 2.5 สามารถแทรกซึมลึกถึงถุงลมปอด ก่อ ปอดอักเสบ ระดับเซลล์ เพิ่ม oxidative stress และเร่งความเสียหายของ DNA จนเกิดการเปลี่ยนแปลงของยีนที่เกี่ยวข้องกับการเจริญเติบโตของเซลล์ นี่คือเหตุผลว่าทำไม มะเร็งปอด และโรคทางเดินหายใจเรื้อรังจึงเพิ่มขึ้น แม้ในผู้ที่ไม่สูบบุหรี่

กลไกของ PM 2.5 ในการทำร้ายร่างกายและก่อมะเร็ง: จากการอักเสบเรื้อรังสู่การกลายพันธุ์ของยีนและมะเร็งปอด**
PM 2.5 ไม่ได้เป็นเพียง “ฝุ่นขนาดเล็ก” ที่ก่อการระคายเคืองชั่วคราว แต่เป็นปัจจัยก่อโรคเชิงระบบ (systemic pathogenic factor) ที่สามารถเปลี่ยนแปลงสภาวะชีววิทยาของร่างกายในระยะยาว โดยเฉพาะในปอดซึ่งเป็นด่านแรกของการสัมผัส กลไกการทำร้ายร่างกายและการก่อมะเร็งของ PM 2.5 สามารถอธิบายได้อย่างเป็นลำดับขั้นดังต่อไปนี้
1) การเข้าสู่ถุงลมปอดและการกระตุ้นภูมิคุ้มกันประจำถิ่น (Local immune activation)
ด้วยขนาดที่เล็กมาก PM 2.5 สามารถหลุดผ่านระบบกรองตามธรรมชาติของทางเดินหายใจส่วนต้น และลงสู่ระดับ ถุงลมปอด (alveoli) ได้โดยตรง เมื่ออนุภาคเหล่านี้สัมผัสกับเซลล์เยื่อบุถุงลมและเซลล์ภูมิคุ้มกันประจำถิ่น (เช่น macrophage) จะเกิดการรับรู้สิ่งแปลกปลอมผ่านตัวรับจำพวก pattern-recognition receptors ทำให้เซลล์ถูกกระตุ้นให้เข้าสู่ภาวะอักเสบ ผลลัพธ์สำคัญคือ การกระตุ้น macrophage ให้หลั่งสารก่อการอักเสบ การดึงดูดเซลล์อักเสบเพิ่มเติมเข้าสู่เนื้อปอด การเปลี่ยน microenvironment ของปอดจากภาวะสมดุล ไปสู่ภาวะอักเสบอย่างต่อเนื่อง ขั้นตอนนี้คือ “จุดเริ่มต้น” ของกระบวนการก่อโรคทั้งหมดจาก PM 2.5
2) การเกิดการอักเสบเรื้อรัง (Chronic inflammation) ซึ่งไม่แสดงอาการชัดเจน
ความอันตรายของ PM 2.5 คือมันไม่ได้กระตุ้นการอักเสบแบบรุนแรงเฉียบพลันเพียงครั้งเดียว แต่ก่อให้เกิด การอักเสบระดับต่ำแต่ต่อเนื่อง (low-grade chronic inflammation) ซึ่งผู้ป่วยมักไม่รู้สึกเจ็บป่วยชัดเจน ในระดับชีวโมเลกุล การอักเสบเรื้อรังนี้สัมพันธ์กับ การหลั่งไซโตไคน์อักเสบ เช่น IL-6, TNF-α, IL-1β การกระตุ้นสัญญาณอักเสบภายในเซลล์อย่างต่อเนื่อง การรบกวนการควบคุมวงจรเซลล์และการซ่อมแซมเนื้อเยื่อ การอักเสบเรื้อรังจึงเปรียบเสมือน “ไฟอ่อนที่ไม่ดับ” ซึ่งค่อย ๆ ทำลายโครงสร้างและการทำงานของปอดในระยะยาว
3) การเพิ่มอนุมูลอิสระและภาวะ Oxidative stress (ROS/RNS overload)
PM 2.5 มีคุณสมบัติในการเพิ่มการสร้าง อนุมูลอิสระ (Reactive Oxygen Species; ROS) และ Reactive Nitrogen Species (RNS) ทั้งจาก องค์ประกอบภายในอนุภาคฝุ่น (โลหะหนัก สารอินทรีย์จากการเผาไหม้) การกระตุ้นการทำงานของเซลล์อักเสบที่สร้าง ROS/RNS ภาวะ oxidative stress ที่เกิดขึ้นส่งผลต่อ เยื่อหุ้มเซลล์ (lipid peroxidation) ไมโตคอนเดรีย (พลังงานของเซลล์) โปรตีนและเอนไซม์ และที่สำคัญที่สุดคือ DNA เมื่อ ROS/RNS สูงเกินขีดความสามารถของระบบต้านอนุมูลอิสระตามธรรมชาติ ความเสียหายระดับโมเลกุลจะสะสมอย่างหลีกเลี่ยงไม่ได้
4) ความเสียหายของ DNA และความไม่เสถียรของจีโนม (Genomic instability)
การทำลาย DNA จาก PM 2.5 ไม่จำเป็นต้องรุนแรงในครั้งเดียว แต่เกิดซ้ำ ๆ จาก oxidative stress และการอักเสบเรื้อรัง ส่งผลให้ เกิด DNA strand break เกิด base modification เกิดความผิดพลาดระหว่างการซ่อมแซม DNA เมื่อระบบซ่อมแซมทำงานหนักและต่อเนื่อง ความผิดพลาดเล็ก ๆ จะเริ่มสะสม กลายเป็น genomic instability ซึ่งเป็นพื้นฐานสำคัญของการเกิดมะเร็ง
5) การคัดเลือกเซลล์ผิดปกติภายใต้แรงกดดันจากสิ่งแวดล้อม (Clonal selection)
PM 2.5 ไม่เพียงทำให้เกิดความเสียหาย แต่ยังสร้าง “สนามคัดเลือก” ให้เซลล์ที่สามารถอยู่รอดภายใต้สภาวะอักเสบและ oxidative stress ได้ดีกว่า ขยายตัวมากกว่าเซลล์ปกติ เซลล์ลักษณะนี้มักมีคุณสมบัติ เช่น แบ่งตัวเร็ว ดื้อการตายของเซลล์ (apoptosis resistance) พึ่งพาสัญญาณการเจริญเติบโตสูง กระบวนการนี้เป็นหัวใจของการที่ PM 2.5 ทำหน้าที่เป็น tumor promoter มากกว่าสารก่อมะเร็งแบบเฉียบพลัน
6) การกระตุ้นสัญญาณการเจริญเติบโตและการกลายพันธุ์ของยีนสำคัญ (เช่น EGFR)
ภายใต้สภาวะอักเสบเรื้อรังและ oxidative stress สัญญาณการเจริญเติบโตของเซลล์จะถูกกระตุ้นอย่างต่อเนื่อง โดยเฉพาะเส้นทางที่เกี่ยวข้องกับ การแบ่งตัวของเซลล์ การอยู่รอด การเคลื่อนที่และการลุกลาม เซลล์ที่มีการเปลี่ยนแปลงของยีนในกลุ่มนี้จะได้เปรียบเชิงชีววิทยา ทำให้ ขยายตัวได้ดีกว่า สะสมความผิดปกติมากขึ้น พัฒนาไปสู่ มะเร็งปอดในผู้ไม่สูบบุหรี่ ได้ในที่สุด นี่คือเหตุผลที่ PM 2.5 เชื่อมโยงกับมะเร็งปอดชนิดที่พบในคนเมืองและผู้หญิงมากขึ้นในปัจจุบัน
7) ผลกระทบเชิงระบบ: ทำไม PM 2.5 จึงเกี่ยวข้องกับมะเร็งหลายอวัยวะ
PM 2.5 บางส่วนสามารถเข้าสู่กระแสเลือด ทำให้เกิด การอักเสบระดับระบบ (systemic inflammation) oxidative stress ทั่วร่างกาย การรบกวนสมดุลภูมิคุ้มกันและฮอร์โมน ด้วยเหตุนี้ ผลกระทบของ PM 2.5 จึงไม่จำกัดอยู่ที่ปอดเพียงอย่างเดียว แต่มีความเกี่ยวข้องกับมะเร็งและโรคเรื้อรังในอวัยวะอื่น ๆ ผ่านกลไกการอักเสบและความเสียหายระดับโมเลกุลร่วมกัน
“กลไกของตำรับสมุนไพร KERRA ในการยับยั้งการอักเสบ ลด ROS Detox ปอด และยับยั้งแกน EGFR–MAPK: การวิเคราะห์เชิงโปรตีโอมิกและงานวิจัยในหลอดทดลอง
ตำรับสมุนไพร KERRA เป็นตำรับยาโบราณตามคัมภีร์ “ตักศิลา” ที่มีกลไกการออกฤทธิ์ในรูปแบบของ “เวชศาสตร์เชิงระบบ” (systems medicine) ไม่ใช่การออกฤทธิ์เฉพาะจุดเพียงเป้าหมายเดียว แต่เป็นการ ปรับสมดุลเครือข่ายชีวโมเลกุลที่ถูกรบกวนจาก PM 2.5 ซึ่งงานวิจัยที่คุณแนบมา ทั้งระดับเซลล์ ระดับเอนไซม์ และระดับโปรตีนที่ตรวจสอบได้จาก proteomics แสดงภาพเดียวกันอย่างสอดคล้องว่า KERRA ทำงานผ่านหลายแกนพร้อมกัน
KERRA กับการยับยั้งการอักเสบเชิงลึก (Anti-inflammatory network modulation)
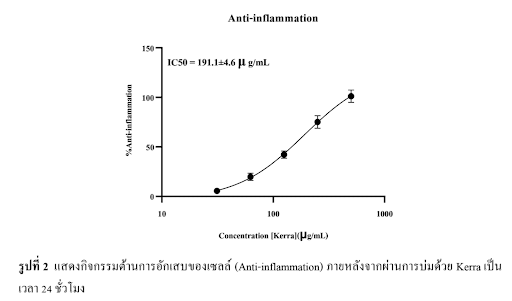
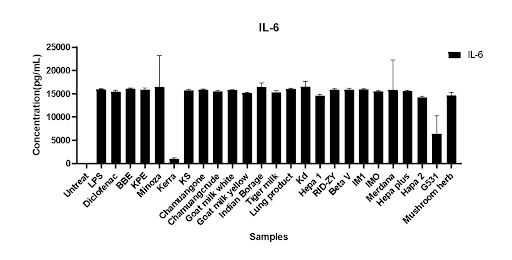
PM 2.5 สร้างการอักเสบเรื้อรังผ่าน macrophage–epithelial crosstalk และไซโตไคน์หลัก เช่น IL-6, TNF-α, IL-1β งานวิจัยในโมเดล RAW264.7 macrophage + LPS แสดงให้เห็นชัดว่า KERRA ลด NO (nitric oxide) ลงใกล้ระดับเซลล์ปกติ (untreated) ลด IL-6 ได้เด่นชัดที่สุดในกลุ่มสารทดสอบทั้งหมด ไม่ก่อพิษต่อเซลล์ภูมิคุ้มกัน (cell viability สูง) ในเชิงกลไก สิ่งนี้สะท้อนว่า KERRA ตัดวงจรการอักเสบตั้งแต่ต้นน้ำ โดยยับยั้งการทำงานของ macrophage ที่ถูกกระตุ้นเกินจาก PM 2.5 ซึ่งเป็นแหล่งกำเนิด “ไฟอักเสบ” หลักของปอดเรื้อรัง
การลด Oxidative stress และบทบาท Detox ปอดในระดับเซลล์
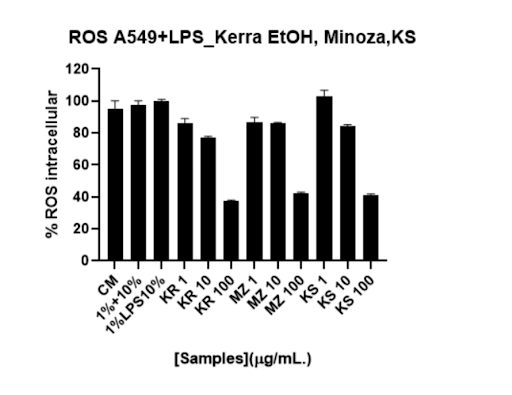
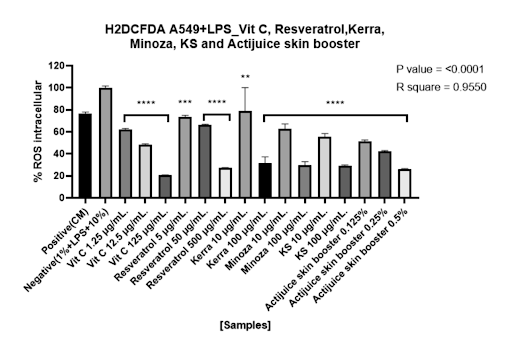
PM 2.5 สร้างการอักเสบเรื้อรังผ่าน macrophage–epithelial crosstalk และไซโตไคน์หลัก เช่น IL-6, TNF-α, IL-1β งานวิจัยในโมเดล RAW264.7 macrophage + LPS แสดงให้เห็นชัดว่า KERRA ลด NO (nitric oxide) ลงใกล้ระดับเซลล์ปกติ (untreated) ลด IL-6 ได้เด่นชัดที่สุดในกลุ่มสารทดสอบทั้งหมด ไม่ก่อพิษต่อเซลล์ภูมิคุ้มกัน (cell viability สูง) ในเชิงกลไก สิ่งนี้สะท้อนว่า KERRA ตัดวงจรการอักเสบตั้งแต่ต้นน้ำ โดยยับยั้งการทำงานของ macrophage ที่ถูกกระตุ้นเกินจาก PM 2.5 ซึ่งเป็นแหล่งกำเนิด “ไฟอักเสบ” หลักของปอดเรื้อรัง
PM 2.5 เพิ่ม ROS/RNS อย่างต่อเนื่อง ทำให้ระบบ detox และ antioxidant ของปอดทำงานหนัก งานวิจัยในเซลล์ปอด A549 + LPS (ROS assay ด้วย H2DCFDA) แสดงว่า KERRA ลด ROS แบบ dose-dependent ลด ROS ลงอย่างมีนัยสำคัญเมื่อเพิ่มความเข้มข้น ทำได้โดยไม่ทำลายเซลล์ปอด (ไม่เกิด cytotoxicity) ในมุมมองเชิงระบบ การลด ROS ไม่ใช่เพียง “ต้านอนุมูลอิสระ” แต่คือการลด DNA damage burden ลดการกระตุ้น NF-κB / MAPK ลดการเร่งการกลายพันธุ์ของยีนในระยะยาว นี่คือความหมายของคำว่า “detox ปอด” ในเชิงชีววิทยา ไม่ใช่การล้างสารพิษแบบผิวเผิน แต่เป็นการลดภาระ oxidative stress ที่เซลล์ต้องเผชิญทุกวันจาก PM 2.5
การกดสวิตช์กลาง NF-κB และ MAPK: หัวใจของการยับยั้งโรคเรื้อรัง
ข้อมูล Western blot (A549 + LPS) แสดงให้เห็นว่า KERRA ลดการแสดงออกของ phosphorylated NF-κB (p65) NF-κB คือ master regulator ที่เชื่อม PM 2.5 ทำให้เกิดการอักเสบเรื้อรัง การอยู่รอดของเซลล์ผิดปกติ และก่อให้เกิดมะเร็ง การกด NF-κB หมายถึง ลดการสร้างไซโตไคน์อักเสบ ลดการกระตุ้น MAPK downstream ลดสภาวะ “pro-tumor microenvironment” ของปอด จุดนี้มีความสำคัญมาก เพราะ PM 2.5 ไม่ได้ก่อมะเร็งด้วยการทำลาย DNA เพียงอย่างเดียว แต่สร้าง “สภาพแวดล้อมเลี้ยงมะเร็ง” และ KERRA แสดงศักยภาพในการทำให้สภาพแวดล้อมนั้น “สงบลง”
KERRA กับการยับยั้งยีนและโปรตีนที่เกี่ยวข้องกับ EGFR-driven carcinogenesis
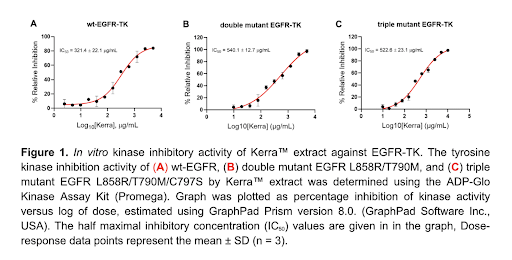
งานวิจัยระดับเอนไซม์และเซลล์แสดงว่า KERRA สามารถ ยับยั้ง EGFR tyrosine kinase ได้ทั้ง wild-type EGFR double-mutant (L858R/T790M) triple-mutant (L858R/T790M/C797S) ในบริบทของ PM 2.5 สิ่งนี้มีนัยสำคัญอย่างยิ่ง เพราะ PM 2.5 กระตุ้น EGFR signaling ทางอ้อมผ่านการอักเสบและ ROS EGFR pathway เป็นเส้นทางหลักที่ทำให้เซลล์ปอด “อยู่รอดและขยายตัว” การยับยั้ง EGFR โดยไม่ต้องรอให้เกิดมะเร็งเต็มรูปแบบ คือหัวใจของการป้องกัน
การวิเคราะห์เชิงโปรตีโอมิกส์: ภาพรวมเชิงระบบของผล KERRA
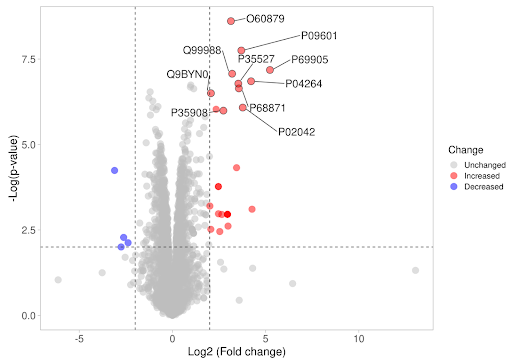
ข้อมูล proteomics (จากงาน Medicina) สนับสนุนแนวคิดว่า KERRA ไม่ได้ยับยั้งโปรตีนตัวเดียว แต่ปรับเครือข่ายโปรตีนที่เกี่ยวข้องกับ การอักเสบ (inflammatory proteins) oxidative stress response cell survival / apoptosis balance cytoskeleton & migration proteins ผลที่เห็นจาก proteomics และ FTIR สอดคล้องกัน คือ โปรไฟล์ชีวโมเลกุลของเซลล์ที่ได้รับ KERRA แตกต่างจากยามุ่งเป้าแบบเดี่ยว เซลล์ถูกปรับเข้าสู่โหมด “ควบคุมและฟื้นฟู” มากกว่า “ถูกบังคับฆ่า” ลดสัญญาณที่เอื้อต่อการลุกลามและการแพร่กระจาย
นี่คือจุดแข็งเชิงชีววิทยาของตำรับสมุนไพรแบบผสม (polyherbal formulation)

KERRA กับการปกป้อง DNA: ต้านการทำลาย DNA และกระตุ้นกระบวนการซ่อมแซม DNA ในระดับโปรตีโอมิกส์
ปัญหา PM 2.5 ไม่ได้ทำร้ายปอดเพียงแค่ก่อปอดอักเสบ หรือปอดอุดกั้นเรื้อรัง เท่านั้น แต่ยังเป็นต้นเหตุสำคัญของ DNA damage ซึ่งเป็นจุดเริ่มต้นของการกลายพันธุ์และการเกิด มะเร็งปอด รวมถึงมะเร็งชนิดอื่น ๆ ในยุคมลพิษ งานวิจัยสมัยใหม่ยืนยันว่าอนุมูลอิสระจาก PM 2.5 (โดยเฉพาะ •OH จากปฏิกิริยาแบบ Fenton) ทำลายโครงสร้าง DNA อย่างรุนแรง หากไม่ถูกยับยั้งหรือซ่อมแซม จะเร่งกระบวนการก่อมะเร็งในระยะยาว
1) PM 2.5 ทำลาย DNA ได้อย่างไร: กลไกชีวเคมีที่ต้องหยุด
เมื่อร่างกายสัมผัส PM 2.5 อนุภาคฝุ่นและโลหะหนักจะกระตุ้นการเกิดอนุมูลอิสระจำนวนมาก โดยเฉพาะ hydroxyl radical (•OH) ซึ่งมีฤทธิ์แรงต่อ DNA กลไกสำคัญประกอบด้วย Oxidative stress overload: ROS/RNS ทำให้เกิด DNA strand break และ base modification Fenton chemistry: Fe²⁺ + H₂O₂ → •OH ทำลาย DNA โดยตรง Inflammation-driven damage: การอักเสบเรื้อรังเพิ่มโอกาสซ่อมแซมผิดพลาด ผลลัพธ์คือ genomic instability และการคัดเลือกเซลล์ผิดปกติสู่มะเร็ง
2) หลักฐานเชิงทดลอง: KERRA ยับยั้งการทำลาย DNA
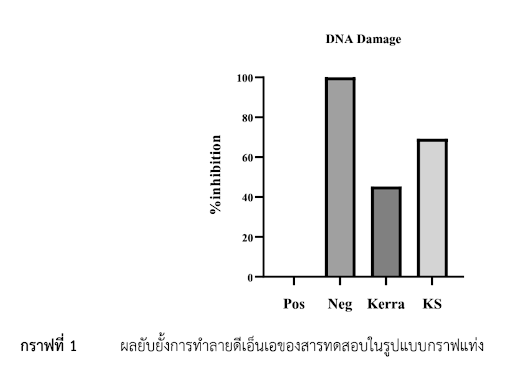
การทดสอบ DNA Damage (Fenton Reagent Assay) การทดลองใช้ Fenton Reagent (Fe²⁺ + H₂O₂) เพื่อสร้าง •OH ทำลาย DNA แล้วประเมินการยับยั้งด้วย Agarose gel electrophoresis ผลการทดสอบระบุชัดว่า KERRA 1 μg/mL ยับยั้งการทำลาย DNA ได้ 45% KS 1 μg/mL ยับยั้งการทำลาย DNA ได้ 69% เมื่อเทียบกับกลุ่มควบคุม (Positive control = 0%, Negative control = 100%) ข้อมูลนี้ยืนยันว่า KERRA มีฤทธิ์ปกป้อง DNA จากอนุมูลอิสระที่รุนแรง อย่างมีนัยสำคัญ แม้ใช้ความเข้มข้นต่ำมาก
3) จากการปกป้อง DNA สู่การซ่อมแซม DNA: มุมมองระดับโปรตีโอมิกส์
การป้องกัน DNA ที่ยั่งยืนไม่ใช่เพียงหยุดการทำลาย แต่ต้อง เสริมระบบซ่อมแซม ด้วย การวิเคราะห์ proteomics (จากชุดข้อมูลเสริมของงานวิจัย) แสดงให้เห็นว่า KERRA มีอิทธิพลต่อเครือข่ายโปรตีนที่เกี่ยวข้องกับการตอบสนองต่อ oxidative stress การควบคุมการอักเสบ สมดุล survival–apoptosis ซึ่งเป็นสภาพแวดล้อมที่เอื้อต่อการซ่อมแซม DNA อย่างมีประสิทธิภาพ
4) Nrf2: แกนกลางของการป้องกันและซ่อมแซม DNA
Nrf2 (Nuclear factor erythroid 2–related factor 2) เป็น transcription factor หลักที่ควบคุมยีนต้านอนุมูลอิสระและการป้องกันเซลล์ กระตุ้นเอนไซม์ต้าน ROS (เช่น NQO1, HO-1)ลดการอักเสบเรื้อรัง ปกป้อง DNA และลดโอกาสกลายพันธุ์ สนับสนุนการกำจัดเซลล์เสียหาย (apoptosis) อย่างเหมาะสม จากข้อมูล pathway analysis การที่ KERRA ปรับเครือข่ายที่เกี่ยวข้องกับ Nrf2 ชี้ว่า KERRA อาจเสริมการป้องกัน DNA และเอื้อต่อการซ่อมแซม DNA ในระดับระบบ ซึ่งสอดคล้องกับผลการยับยั้ง DNA damage ที่วัดได้จริง
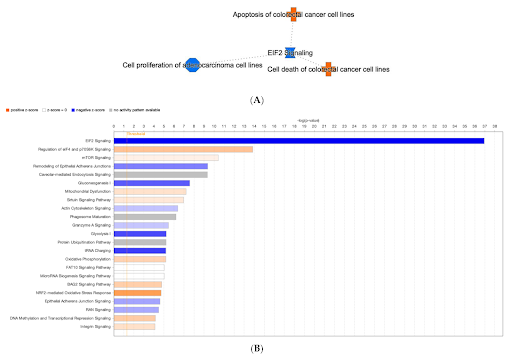
5) เชื่อมโยงสู่การป้องกันมะเร็งปอดจาก PM 2.5
การป้องกันมะเร็งปอดในยุค PM 2.5 ต้องตัดวงจร 3 ชั้นพร้อมกัน หยุด DNA damage (ยับยั้ง •OH/ROS) ลดการอักเสบเรื้อรัง (ลดแรงคัดเลือกคลอนผิดปกติ) เสริมการซ่อมแซม DNA (ผ่านเครือข่าย antioxidant & repair) หลักฐานจาก Fenton assay + proteomics/pathway analysis แสดงว่า KERRA ตอบโจทย์ทั้งสามชั้น จึงเหมาะกับการใช้เชิงป้องกันระยะยาวในกลุ่มเสี่ยง PM 2.5

สรุปกลไกของ KERRA จากงานวิจัยทั้งหมด (ภาพรวมเชิงระบบ)
เมื่อบูรณาการข้อมูลทุกการทดลอง สามารถสรุปกลไกของ KERRA ต่อ PM 2.5 ได้ดังนี้
- ยับยั้งต้นน้ำการอักเสบ
- ลด NO, IL-6 จาก macrophage
- ลด oxidative stress และ detox ปอดในระดับเซลล์
- ลด ROS ในเซลล์ปอด
- กดสวิตช์กลางของโรคเรื้อรัง
- ยับยั้ง NF-κB และ MAPK signaling
- ยับยั้งแกนมะเร็งโดยตรง
- ยับยั้ง EGFR-TK (WT และ mutant)
- ปรับสมดุลเครือข่ายโปรตีน (proteomics)
- ลดสัญญาณอยู่รอด/ลุกลาม
- สนับสนุนสมดุล apoptosis–repair
กล่าวโดยสรุป KERRA ทำหน้าที่เป็น “network protector” ของปอดในยุค PM 2.5
มากกว่าสารต้านอักเสบหรือสารต้านมะเร็งแบบเดี่ยว
เอกสารอ้างอิง
- World Health Organization. Ambient air pollution: A global assessment of exposure and burden of disease. WHO Press; 2016.
- International Agency for Research on Cancer (IARC). Outdoor air pollution. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. Vol 109. Lyon: IARC; 2016.
- Cohen AJ, Brauer M, Burnett R, Anderson HR, Frostad J, Estep K, et al. Estimates and 25-year trends of the global burden of disease attributable to ambient air pollution. Lancet. 2017;389(10082):1907–18.
- Schraufnagel DE, Balmes JR, Cowl CT, De Matteis S, Jung SH, Mortimer K, et al. Air pollution and noncommunicable diseases. Chest. 2019;155(2):409–16.
- Turner MC, Andersen ZJ, Baccarelli A, Diver WR, Gapstur SM, Pope CA 3rd, et al. Outdoor air pollution and cancer: An overview of the current evidence. CA Cancer J Clin. 2020;70(6):460–79.
- Bauer AK, Velmurugan K, Xiong KN, Alexander CM. Mechanisms of air pollution-induced lung cancer. Carcinogenesis. 2022;43(1):1–10.
- Kelly FJ, Fussell JC. Air pollution and airway disease. Clin Exp Allergy. 2011;41(8):1059–71.
- Li R, Zhou R, Zhang J. Function of PM2.5 in the pathogenesis of lung cancer and chronic airway inflammatory diseases. Oncol Lett. 2018;15(5):7506–14.
- Guo H, Zhang Z, Zhang Y, Chen X, Li L. PM2.5 exposure induces lung inflammation through TLR4/NF-κB signaling pathway. Ecotoxicol Environ Saf. 2021;222:112540.
- Karin M, Greten FR. NF-κB: Linking inflammation and immunity to cancer development and progression. Nat Rev Immunol. 2005;5(10):749–59.
- Mantovani A, Allavena P, Sica A, Balkwill F. Cancer-related inflammation. Nature. 2008;454(7203):436–44.
- Kensler TW, Wakabayashi N, Biswal S. Cell survival responses to environmental stresses via the Keap1–Nrf2–ARE pathway. Annu Rev Pharmacol Toxicol. 2007;47:89–116.
- Ma Q. Role of Nrf2 in oxidative stress and toxicity. Annu Rev Pharmacol Toxicol. 2013;53:401–26.
- Taguchi K, Motohashi H, Yamamoto M. Molecular mechanisms of the Keap1–Nrf2 pathway in stress response and cancer evolution. Genes Cells. 2011;16(2):123–40.
- Hayes JD, Dinkova-Kostova AT. The Nrf2 regulatory network provides an interface between redox and intermediary metabolism. Trends Biochem Sci. 2014;39(4):199–218.
- Fenton HJH. Oxidation of tartaric acid in presence of iron. J Chem Soc Trans. 1894;65:899–910. (อ้างอิงกลไก Fenton reaction สำหรับ hydroxyl radical)
- Halliwell B, Gutteridge JMC. Free radicals in biology and medicine. 5th ed. Oxford: Oxford University Press; 2015.
- Valko M, Leibfritz D, Moncol J, Cronin MTD, Mazur M, Telser J. Free radicals and antioxidants in normal physiological functions and human disease. Int J Biochem Cell Biol. 2007;39(1):44–84.
- Pao W, Miller V. Epidermal growth factor receptor mutations, small-molecule kinase inhibitors, and non–small-cell lung cancer. J Clin Oncol. 2005;23(11):2556–68.
- Harrison PT, Vyse S, Huang PH. Rare EGFR mutations in non–small cell lung cancer. Semin Cancer Biol. 2020;61:167–79.
- Jänne PA, Yang JC, Kim DW, Planchard D, Ohe Y, Ramalingam SS, et al. AZD9291 in EGFR inhibitor–resistant non–small-cell lung cancer. N Engl J Med. 2015;372(18):1689–99.
- Rangachari D, To C, Shpilsky JE, VanderLaan PA, Kobayashi SS, Mushajiang M, et al. EGFR-mutated lung cancers resistant to osimertinib. J Thorac Oncol. 2019;14(11):1995–2002.
- Chowdhury P, Dey P, Ghosh S, Sarma A, Ghosh U. Inhibition of EGFR/Akt/p38/ERK signaling reduces metastatic potential in NSCLC. BMC Cancer. 2019;19:829.
- งานวิจัยและรายงานเฉพาะของ KERRA / KS
- ห้องปฏิบัติการชีวเคมี มหาวิทยาลัยเกษตรศาสตร์. รายงานผลการทดสอบ DNA Damage ด้วยวิธี Fenton Reagent. 2023.
- Supplementary data. Proteomic pathway analysis of Kerra-treated HCT116 cells. Medicina. 2023.



